Vėžys yra vienas iš labiausiai sudėtingos ir pamokančios žmonių ligosreiškiantis dramatišką normalių ląstelių procesų sutrikimą, kuris leidžia ląstelėms nekontroliuojamai auga, priešinasi mirčiai, įsiskverbia į aplinkinius audinius ir metastazuoja. Su sergamumas vėžiu auga visame pasaulyjesuprasti jo pagrindinius mechanizmus yra labai svarbu studentams, mokslininkams ir gydytojams. Dešimtmečius trukę tyrimai atskleidė, kad vėžį galima suprasti per skirtingos, bet tarpusavyje susijusios konceptualios dimensijosįskaitant:
Įgytos funkcinės galimybės (vėžio požymiai)
Įgalinamos fenotipinės savybės
Požymius pernešančios ląstelės naviko mikroaplinkoje (TME)
Sisteminė sąveika šeimininko viduje
Kartu šie matmenys suteikia a vėžį kaip dinamišką, prisitaikantį „uždraustą organą“ tirtivadovaujantis terapinių strategijų kūrimui.
Įvadas: skiriamųjų ženklų koncepcija
Sąvoka „vėžio požymiai“ buvo pristatytas Douglasas Hanahanas ir Bobas Weinbergas organizuoti didžiulę auglių stebimų genetinių ir fenotipinių pokyčių įvairovę. Tikslas buvo suprasti, kaip atsiranda vėžys daugiapakopė navikogenezėvystosi per selektyvų spaudimą ir įgyja tokių bruožų kaip metastazės, atsparumas terapijai ir imuninės sistemos vengimas.
Požymio evoliucijos laiko juosta:
2000: Šeši požymiai: proliferacinio signalizavimo palaikymas, augimo slopintojų išvengimas, atsparumas ląstelių mirčiai, replikacinis nemirtingumas, angiogenezė, invazija / metastazės.
2011 m.: Pridėta nereguliuojama medžiagų apykaita ir imuniteto vengimas.
2022 m.: Pridėta fenotipinio plastiškumo, pabrėžiant dinamiškas prisitaikymas prie terapijos ir aplinkos.
Centrinis suvokimas buvo tas vien mutantinės vėžio ląstelės neapibrėžia naviko biologijos. Vietoj to, vėžio progresavimas priklauso nuo aplinkinių normalių ląstelių įdarbinimas ir perprogramavimassukuriant a palaikomoji naviko mikroaplinka (TME).
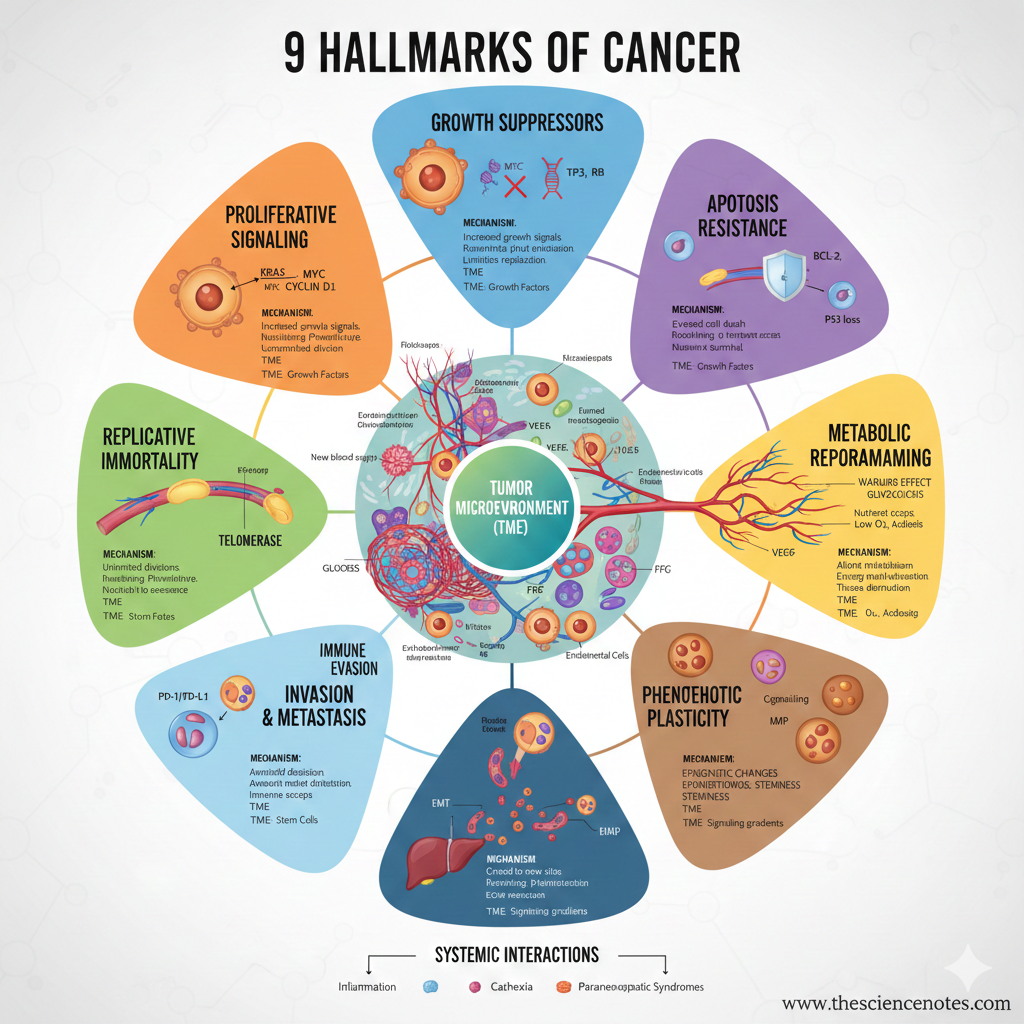
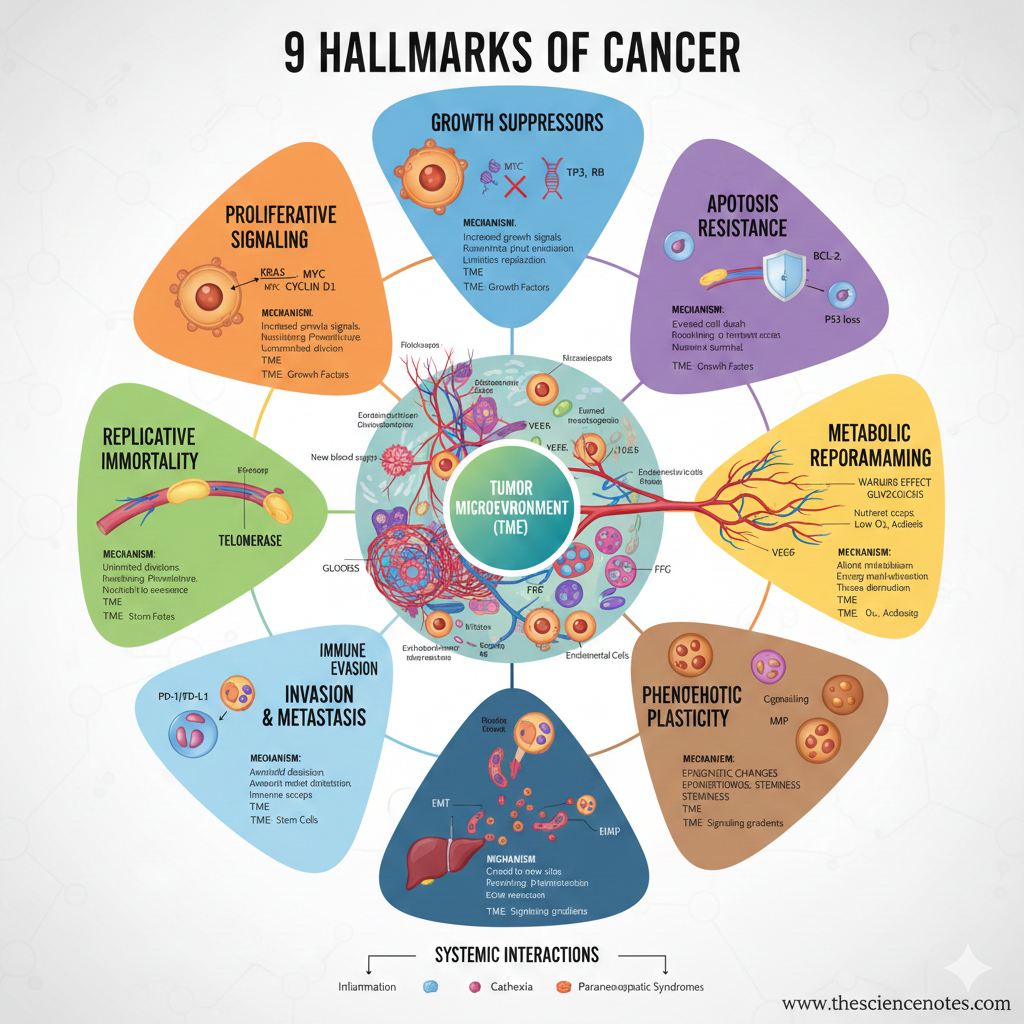
9 vėžio požymiai
1. Proliferacinio signalizavimo palaikymas
Vėžio ląstelės pasiekia nekontroliuojamas platinimas suaktyvinus onkogenųkurie skatina lėtinio ląstelių ciklo progresavimą.
Pagrindiniai onkogenai:
KRAS, NRAS, HRAS: KRAS mutacijos pastebimos ~ 30 % navikų, įskaitant kasos (~ 90 %), gaubtinės ir tiesiosios žarnos (~ 50 %) ir plaučių (~ 35 %) vėžį.
BRAF, PIK3CA, BCR-ABL: Skatinkite nenormalius augimo signalus.
MYC: Transkripcijos faktorius, reguliuojantis tūkstančius genų; amplifikuota ~40% navikų.
Mechanizmai:
Genų amplifikacija arba pertvarkymas
Žiedinė ekstrachromosominė DNR (ecDNR) sustiprina onkogeno ekspresiją
Epigenetinis perprogramavimasįskaitant autokrininio / parakrininio augimo faktoriaus kilpas
Klinikinė reikšmė: Tikslinės terapijos apima BRAF inhibitoriai (vemurafenibas) ir HER2 inhibitoriai (trastuzumabas).
Papildoma įžvalga: RAS ir MYC gali skatinti daugybę kitų skiriamųjų ženklų galimybiųįskaitant medžiagų apykaitos perprogramavimą ir angiogenezę, pabrėžiant jų centrinė naviko evoliucija.
2. Vengti augimo slopintojų
Normalios ląstelės reguliuoja proliferaciją per naviką slopinantys genai (TSG)kurie veikia kaip vartų sargai ląstelių ciklo kontroliniams taškams.
Pagrindinės TSG:
TP53: Suaktyvinamas reaguojant į DNR pažeidimą, onkogeninį stresą arba hipoksiją; reguliuoja apoptozę, senėjimą ir ląstelių ciklo sustabdymą. Mutuoja ~40% vėžio atvejų.
RB, CDKN1A / B (p21 / p27), CDKN2A (p16INK4a / p14ARF): Blokuoti progresą per G1/S ir G2/M perėjimus.
APC: Degraduoja β-kateniną, kad būtų išvengta nekontroliuojamo proliferacijos.
Vengimo mechanizmai:
Klinikinė reikšmė: Narkotikai kaip CDK inhibitoriai (palbociklibas, ribociklibas) gali atkurti auglių augimo slopinimą su GTG inaktyvacija.
3. Pasipriešinimas užprogramuotai ląstelių žūčiai (apoptozei)
Vėžio ląstelės vengia ląstelių savižudybės mechanizmaileidžianti išgyventi nepaisant DNR pažeidimo ar nenormalaus signalo.
Mechanizmai:
Per didelis anti-apoptotinių baltymų ekspresija: BCL-2, BCL-XL, MCL-1
TP53 inaktyvacija, užkertanti kelią proapoptotinių genų, tokių kaip indukcija, indukcijai PUMA ir NOXA
Alternatyvių ląstelių mirties būdų disreguliavimas: nekroptozė, ferroptozė, piroptozė, autofagija
Terapija: BH3 mimetikai (Venetoclax) atkurti apoptozę CLL ir AMLvykstantys kitų vėžio formų tyrimai.
Paradoksali įžvalga: Apoptozinės ląstelės gali stimuliuoja naviko augimą skatinančius signalus gretimose ląstelėse arba išvengti mirties su iš dalies pažeistais genomais, prisidedant prie genomo nestabilumas ir naviko progresavimas.
4. Replikacinio nemirtingumo nustatymas
Normalias ląsteles riboja a mitozinis laikrodis padiktavo telomerų ilgis. Vėžio ląstelės tai apeina dalyti neribotam laikui.
Mechanizmai:
Telomerazės aktyvinimas (TERT): Prideda telomerų pasikartojimų, dažnų sergant glioblastoma (~80%), melanoma (~60%), šlapimo pūslės vėžiu (~80%).
Alternatyvus telomerų pailgėjimas (ALT): Rekombinacija pagrįstas telomero išplėtimas, būdingas mezenchiminiams ir neuroepiteliniams navikams.
Pasekmės:
5. Kraujagyslių indukcija arba prieiga prie jų (angiogenezė)
Augliai reikalauja deguonies ir maistinių medžiagų užaugti daugiau nei 1–2 mm.
Mechanizmai:
Sukelia hipoksiją VEGFA, ANGPT2 ir FGF sekrecija
Endotelio ląstelių aktyvacija, dygimas ir kapiliarų susidarymas
Įdarbinimas pericitai laivo stabilizavimui
Naviko kraujagyslės:
Nesandarus, chaotiškas ir prastai perfuzuotas
Trukdo imuninių ląstelių infiltracijai, prisideda prie imuniteto vengimas
Alternatyvus mechanizmas: Kraujagyslių kooperatyvaskai navikai užgrobia jau esamas kraujagysles, ypač po antiangiogeninio gydymo.
Klinikinė reikšmė: Antiangiogeninis gydymas (pvz. bevacizumabas) nukreiptas į VEGF kelius.
6. Ląstelių metabolizmo reguliavimo panaikinimas
Vėžio ląstelės perprogramuoja medžiagų apykaitą į patenkinti energijos ir biosintezės poreikius.
Metabolizmo strategijos:
Aerobinė glikolizė (Warburg efektas) greta oksidacinis fosforilinimas
Alternatyvių degalų naudojimas: laktatas, glutaminas
Metabolinis kryžminimas su naviko mikroaplinkos ląstelės (fibroblastai, makrofagai, T ląstelės)
TME veiksniai:
Hipoksija, acidozė, maistinių medžiagų gradientai
Metabolitų parakrininė sekrecija
Dinaminės adaptacijos naviko progresavimo ir metastazių metu
Terapinės pasekmės: Nukreipimas į glikolizę arba glutamino metabolizmą gali sutrikdyti naviko augimą.
7. Invazijos ir metastazių aktyvinimas
Vėžio ląstelės įgyja gebėjimą išplito už jų kilmės ribų.
Mechanizmai:
Perėjimas iš epitelio į mezenchiminį (EMT) → judrumas
Ekstraląstelinės matricos remodeliavimas per MMP
Įėjimas į kraujo ar limfos cirkuliacija
Tolimų organų kolonizacija
TME indėlis: Stromos ląstelės ir imuninės ląstelės išskiria veiksnius, palengvinančius invaziją.
Klinikinė svarba: Metastazės sukelia ~ 90% su vėžiu susijusių mirčių.
8. Imuninės sistemos sunaikinimo išvengimas
Navikai išvengia imuninės priežiūros per:
Imuniteto kontrolės punktai (PD-L1, CTLA-4)
Imunosupresiniai citokinai
Naviko kraujagyslių rekonstrukcija, siekiant užkirsti kelią T ląstelių infiltracijai
Terapija: Kontrolinių taškų inhibitoriai (nivolumabas, pembrolizumabas) atkuria T ląstelių aktyvumą.
9. Fenotipinio plastiškumo atrakinimas
Vėžio ląstelės dinamiškai pereiti tarp proliferacinių, invazinių ir vaistams atsparių būsenų.
Reikšmė:
Pavaros atsparumas terapijai, atkrytis ir metastazės
Leidžia prisitaikyti prie kintančio TME ir sisteminio slėgio
Fenotipinių charakteristikų įjungimas
Šios remti skiriamųjų ženklų įsigijimą:
Genominis nestabilumas: pagreitina mutacijas ir naviko evoliuciją
Auglį skatinantis uždegimas: kai kurios imuninės ląstelės skatina augimą
Epigenetinis remodeliavimas ir prisitaikymas prie oksidacinio streso pagerinti išgyvenimą nepalankiomis sąlygomis
Auglio mikroaplinka (TME)
Navikai yra nevienalyčiai „organai” su keliais sąveikaujančiais ląstelių tipais:
Vėžio ląstelės: daugintis ir prisitaikyti
Fibroblastai: pertvarkyti ECM ir išskirti augimo faktorius
Imuninės ląstelės: slopina arba skatina naviko augimą
Kraujagyslės: tiekti maistines medžiagas ir pašalinti atliekas
Vaidmuo: TME prisideda prie augimas, invazija, angiogenezė, imuninės sistemos vengimas, metabolinė adaptacija ir atsparumas terapijai.
Sisteminės sąveikos
Navikai sistemiškai sąveikauja su kūnu, pakeisdami:
Hormonų lygis
Metabolinis balansas
Imuniteto stebėjimas
Poveikis: Sisteminis poveikis turi įtakos naviko progresavimui ir terapiniam atsakui.
Terapinės pasekmės
Veiksmingas vėžio gydymas dažnai reikalauja kelių skiriamųjų ženklų taikymas:
Onkogeno inhibitoriai: KRAS, BRAF, HER2
Naviko slopinimo moduliatoriai: CDK inhibitoriai
Apoptozės aktyvatoriai: BH3 mimetikai
Antiangiogeniniai vaistai: VEGF inhibitoriai
Imunoterapija: kontrolinių punktų inhibitoriai
Metabolizmo inhibitoriai: glikolizės / glutamino taikymas
Kombinuota terapija yra labai svarbu įveikti plastiškumas, prisitaikymas ir atsparumas.
Hanahan, D. ir Weinberg, RA (2011). Vėžio požymiai: kita karta. Ląstelė, 144(5), 646–674. https://doi.org/10.1016/j.cell.2011.02.013
Hanahan, D. (2022). Vėžio požymiai: nauji matmenys. Vėžio atradimas, 12(1), 31–46. https://doi.org/10.1158/2159-8290.CD-21-1059
Hanahan, D. (2026). Vėžio požymiai – tada ir dabar, ir vėliau. Ląstelė. https://doi.org/10.1016/j.cell.2025.12.049




